①为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
②化学药品着火,都要立即用水或泡沫灭火器灭火
③配制一定物质的量浓度的稀硫酸溶液时,量取浓硫酸后的量筒要用蒸馏水洗涤,并把洗涤液转入容量瓶中
④配制一定物质的量浓度的溶液定容时,俯视容量瓶的刻线,会使配制的浓度偏高
⑤向溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,说明一定含有SO42﹣
⑥检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液.
①Na2CO3·10H2O晶体 ②铜 ③硫酸溶液 ④CO2 ⑤熔融NaHSO4 ⑥Ba(OH)2固体 ⑦红褐色的氢氧化铁胶体 ⑧盐酸 ⑨CH3COOH ⑩Al2(SO4)3固体
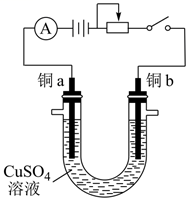
电解前:铜a与铜b的质量分别 和
:
电解后:铜a与铜b的质量分别 和
。
已知: 电子的电量为
,电路中通过的总电量
(t单位为秒)。
则测得的铜元素的相对原子质量为(计算结果保留3位有效数字),写出简要计算过程。
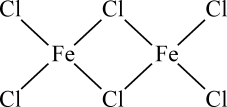 )形式存在,FeCl3的熔点(306℃)是著低于FeF3的熔点(1000℃)的原因是;FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+ , 结构如图所示。在该双核阳离子中,H—O—H键角(填“大于”、“小于”或“等于”)H2O的H—O—H键角;若对FeCl3水溶液进行加热,该对核阳离子内部首先断开的是键(填“a”或“b”)。
)形式存在,FeCl3的熔点(306℃)是著低于FeF3的熔点(1000℃)的原因是;FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+ , 结构如图所示。在该双核阳离子中,H—O—H键角(填“大于”、“小于”或“等于”)H2O的H—O—H键角;若对FeCl3水溶液进行加热,该对核阳离子内部首先断开的是键(填“a”或“b”)。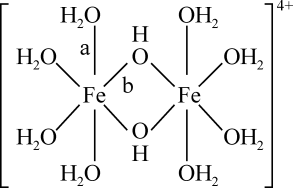
a.离子键|b.氢键 c.配位键 d.金属键
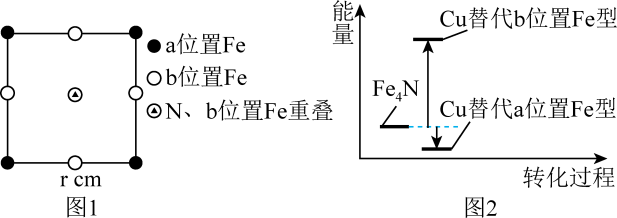
选项 | 物质(括号内为杂质) | 除杂试剂、方法 |
A |
| 加入稀硝酸,溶解、过滤、洗涤、干燥 |
B | 依次通入饱和 | |
C |
| 加入过量 |
D | 乙醇蒸气 | 依次通入酸性高锰酸钾溶液、无水 |
②673K时,合成氨反应机理中各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。
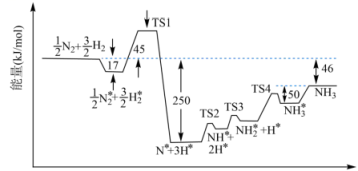
图中决速步骤的反应方程式为。
①
②
写出NH3还原NO至N2和水蒸气的热化学方程式。
。已知该反应的正、逆反应速率方程分别为
、
, 其中
、
分别为正、逆反应速率常数,变化曲线如左下图所示,则该反应的反应热
O(填“>”、“<”或“=”),写出推理过程
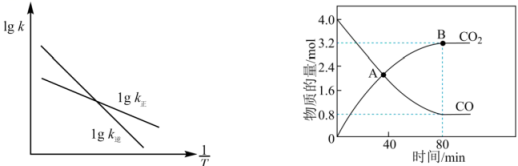
①在A点时,N2O的生成速率N2的生成速率(填“>”、“<”或“=”)。
②若平衡时总压强为p kPa,用平衡分压代替其平衡浓度表示的化学平衡常数(平衡分压=总压×物质的量分数)。
反应原理为KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O=2I-+S4O
步骤如下:
步骤①称取20.000g市售食盐,在容量瓶中配制成100mL溶液;
步骤②取所配溶液25.00mL于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液。
步骤③向锥形瓶中滴加指示剂,用Na2S2O3溶液滴定步骤②所得溶液。平行滴定3次。
选出正确操作并排序检查是否漏水→蒸馏水洗涤→→→a→→→。
a.加液至“0”刻度以上2~3mL处
b.调整液面至“0”刻度或“0”刻度下方,记录读数V₁
c.倾斜转动滴定管,使标准液润湿滴定管内壁,将润洗液从下口排出
d.赶出尖嘴部分气泡
e.向碱式滴定管中加3~5mLNa2S2O3标准液
f.向酸式滴定管中加3~5mLNa2S2O3标准液
g.左手控制活塞(或挤压玻璃珠),右手振荡锥形瓶
h.左手振荡锥形瓶,右手控制活塞(或挤压玻璃珠)
① 转化为
属于(填“化学”或“物理”)变化;
②同温同压下,等质量的 和
的分子数之比为,密度之比为;
③1.6g 和
的混合气体中含有氧原子的数目为(用
表示阿伏加德罗常数的值)。
①废水中一定没有的离子是(填离子符号)。
②向废水中加过量浓氢氧化钠溶液,可能出现的现象是。
③为确定废水中还可能存在的以上离子,具体的实验方法是将少量废水放入试管中,向其中加入稀硝酸至不再产生气体,然后再。
2006-2024 深圳市思高达科技有限公司 粤ICP备14099982号 粤公网安备 44030702004423号



