| 金属 | Na | K | Al | Cu | Fe |
| 熔点/℃ | 97.8 | 63.6 | 660 | 1083 | 1535 |
| 沸点/℃ | 883 | 774 | 2200 | 2595 | 2750 |
 B .
B .  C .
C .  D .
D . 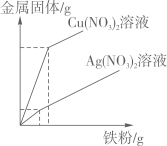
 B .
B .  C .
C .  D .
D . 

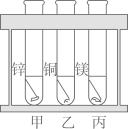
①Na、Mg、Zn三种金属都能置换出酸中的氢
②生成相同质量的氢气消耗金属的质量为Na>Mg=Zn
③生成相同质量的氢气消耗Na、Mg、Zn三种金属的质量比为23∶24∶65
④生成相同质量的氢气消耗Na、Mg、Zn三种金属的原子个数比为2∶1∶1


为结构的主要成分或材料:

| 结构 | 主要成分或材料 |
| 把手 | 金属合金 |
| 车胎 | 合成橡胶 |
| 外壳 | 合成塑料 |
| 电池 | Li、MnO2、电解质溶液 |
|
金属 |
Cr |
Mg |
Cu |
|
与盐酸反应现象 |
放出气泡速率缓慢 |
放出气泡速率较快 |
无明显现象 |
①上述三种金属的活动性由强到弱的顺序是。
②从上述探究实验可知,Cr(填“能”或“不能”)跟CuSO4溶液反应。若反应,请写出反应的化学方程式。
|
金属 |
锡 |
铅 |
锑 |
|
熔点/℃ |
232 |
327 |
630 |

实验Ⅱ:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是〔填写序号)。
①A13+②A13+、Fe2+③A13+、Fe3+④Fe2+、Cu2+⑤A13+、Fe2+、Cu2+
材料一:我国晋代炼丹家葛洪用铁勺盛满曾青(硫酸铜溶液),几天后,铁勺表面红光闪闪,记载为“点铁成金”的故事,后来演变成湿法炼铜法。
材料二:贝采利乌斯是最早为金属活动性排序的科学家,他依靠定性的推测,对元素的电化次序排序为:Ag,Cu,Zn,Mg,Na,Na的电正性最强,Ag的电负性最强,但是设备落后无法定量实验,因此难以准确描述,他自己也认为排序不够准确。
材料三:1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。
材料四:1865年贝开托夫设想找到一种参比物使金属与之发生作用,看反应的难易程度来判断金属活动性的强弱。他以硫酸铜为参比物,铁能跟硫酸铜溶液反应,银不能跟硫酸铜溶液反应,得出铁金属的活动性比银强,从而得出大部分金属活动性强弱。现代科学家发现,金属活动性排序还与反应的条件有关。
|
常见铁的氧化物 |
FeO |
Fe2O3 |
Fe3O4 |
|
能否被磁铁吸引 |
否 |
否 |
能 |
|
与盐酸反应的产物 |
FeCl2和H2O |
FeCl3和H2O |
FeCl2、FeCl3和H2O |
【查阅资料】钠常温下就能与水发生剧烈反应,反应的化学方程式为2Na+2H2O=2NaOH+H2↑。
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成。
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表中所示。
|
实验编号 |
钠块大小 |
硫酸铜溶液 |
实验中产生沉淀的现象 |
|
① |
绿豆大小 |
稀溶液10mL |
产生蓝绿色沉淀 |
|
② |
绿豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀 |
|
③ |
豌豆大小 |
稀溶液10mL |
产生蓝色絮状沉淀 |
|
④ |
豌豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀,并出现黑色固体 |
小科咨询老师后得知蓝绿色沉淀为碱式铜盐。
【实验结论】
【实验反思】实验中生成氢氧化铜沉淀的原理是(用化学方程式表示)。

Ⅰ.Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
Ⅱ.2Cu+O22CuO CuO+H2SO4=CuSO4+H2O
从两种途径可以看出,通常情况下不反应的两种物质,在改变和后,也可以发生反应。相对于第二种方法,第一种方法的不足之处是(写两点)。


【方案】取四支试管编号为①、②、③、④,分别作如图处理,两周后,观察铁钉表面的锈蚀情况。
【分析】
【解释】根据以上实验,请解释学校铁栅栏涂漆能防锈的原因是:。
I.常温下,空气中的氮气和稀有气体不会与镁发生反应。
II.无水CaCl2固体有较强的吸水性,能吸收空气中的水蒸气。
为探究镁表面黑色物质的成因是与空气中的哪些成分有关,他开展如图实验进行探究。

数日后第①组镁条表面出现黑色物质,第②、③组只观察到镁条表面变暗,并没有出现黑色物质。
|
实验编号 |
双氧水质量 |
加入固体物质 |
产生气体的体积 |
耗时 |
结束后固体质量(滤出后烘干) |
|
1 |
100g |
/ |
32mL |
380S |
/ |
|
2 |
100g |
0.2g二氧化锰 |
32mL |
36.5S |
0.2g |
|
3 |
100g |
0.2g氧化铁 |
32mL |
89.5S |
0.2g |