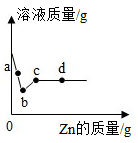
①取少量硫酸铜溶液于试管A中,将铁片(足量)插入硫酸铜溶液中,充分反应后将铁片取出,观察到的实验现象是.
②(请补充实验具体操作).
③取少量硫酸铜溶液于试管B中,将铝片插入硫酸铜溶液中,充分反应,写出该反应的化学方程式.
结论:三种金属的活泼性由强到弱顺序是.
a、齿轮表面涂油 b、将钢材深埋保存
c、将钢刀浸泡在盐水中 d、车圈镀铬.

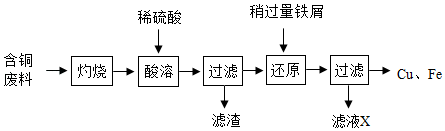
注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
下列关于该流程的说法,错误的是____。
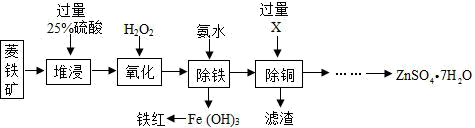
|
编号 |
反应温度/℃ |
溶液 pH |
除铁率/% |
|
a |
30 |
2 |
91.5 |
|
b |
30 |
2.5 |
93.3 |
|
c |
40 |
2.5 |
95.1 |
|
d |
40 |
3.1 |
Y |
|
e |
50 |
3.1 |
99.5 |
①实验对比,得到的结论为其他条件不变时,反应温度增大,除铁率提高。
②实验 a 和实验 b 对比,得到结论是。
③最佳的除铁条件为反应温度℃,溶液 pH。
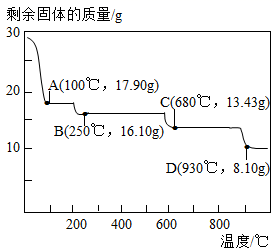
ZnSO4•7H2O 加热到 100℃时所得固体的化学式为是(写出计算过程)。
微信扫码预览、分享更方便