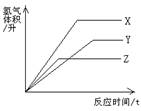
①三种金属与稀硫酸反应,X最剧烈
②反应结束消耗硫酸的质量一定相等
③三种金属的相对原子质量:X>Y>Z
④在同温同压下,产生氢气体积:最大是X
颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
pH范围 | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
 B . 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
B . 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应  C . 等体积,等浓度的双氧水制取氧气
C . 等体积,等浓度的双氧水制取氧气  D . 服用胃舒平[主要成分 Al(OH)3]治疗胃酸过多,胃液 pH 的变化
D . 服用胃舒平[主要成分 Al(OH)3]治疗胃酸过多,胃液 pH 的变化 

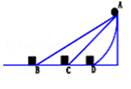
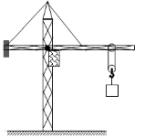

向右运动直至停止。

【查阅资料】①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是(用化学方程式表示)
②K2CO3溶液呈碱性,CaCl2溶液,KCl溶液呈中性。
【猜想假设】假设I:只含KOH;假设II:含KOH和K2CO3;假设III:只含K2CO3。
【进行实验】
|
实验操作步骤 |
实验现象 |
实验结论 |
|
a.取少量样品于试管中,加入足量的稀盐酸 |
有气泡产生 |
假设 错误 |
|
b.另取少量样品于试管中,加水溶解,加入过量的CaCl2 溶液,振荡,静置 |
产生白色沉淀 |
猜想 II 正确 |
|
c.取②中上层清液,滴加无色的酚酞试液 |
|
【拓展应用】完全变质的 KOH 也有利用价值,从K2CO3的组成或性质看,K2CO3在农业上的用 途是 (填一种即可)。
(查阅资料)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2OCO2↑+CO↑+4H2O
碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。为了测定铁红中铁的质量
分数,小组同学进行如下实验。(装置气密性良好,尾气处理装置未画出。)

a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
|
加入稀硫酸的质量 (g) |
充分反应后剩余固体的质量 (g) |
|
|
第 1 次 |
40 |
m |
|
第 2 次 |
40 |
14.8 |
|
第 3 次 |
40 |
12.2 |
|
第 4 次 |
40 |
11.2 |
|
第 5 次 |
40 |
11.2 |
试回答下列问题:
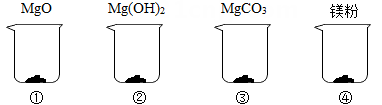
分别取4.2克MgO、Mg(OH)2、MgCO3和“镁粉”置于烧杯中,逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失。四种固体消耗稀盐酸的质量如表所示,且烧杯③和烧杯④中产生了大量气泡。请结合实验现象和数据回答问题。
|
物质 |
MgO |
Mg(OH)2 |
MgCO3 |
“镁粉” |
|
消耗稀盐酸的质量/克 |
121.8 |
m |
58.0 |
61.9 |