| 选项 | A | B | C | D |
| 实验目的 | 证明醋酸溶液呈酸性 | 检验氯离子 | 除去氯化钠溶液中的硫酸钠 | 检验长期露置的氢氧化钠溶液是否变质 |
| 方案一 | 滴加几滴酚酞溶液观察是否变红 | 先加硝酸银溶液,再滴加稀硝酸 | 加入适量的硝酸钡溶液,过滤 | 加稀盐酸 |
| 方案二 | 用pH试纸检验溶液的pH | 先加硝酸银溶液,再滴加稀盐酸 | 加入适量的氯化钡溶液,过滤 | 加澄清石灰水 |


 B . 向一定量的锌粒中不断加入稀硫酸直至过量
B . 向一定量的锌粒中不断加入稀硫酸直至过量  C . 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉
C . 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉  D . 向一定量的氯化铁和氯化钾的混合液中,逐滴加入过量的氢氧化钾溶液
D . 向一定量的氯化铁和氯化钾的混合液中,逐滴加入过量的氢氧化钾溶液 

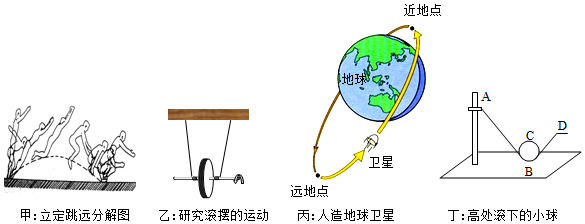
实验次数 | 钢球质量/g | 钢球下摆高度/cm | 木块滑行距离/cm |
1 | 20 | 20 | 30 |
2 | 40 | 20 | 58 |
3 | 60 | 20 |
在第3次实验中,木块被撞后滑出木板,需要重做第3次实验,甲同学建议换用一个较大的木块,乙同学建议换同样材质但较长的木板,丙同学建议降低钢球下摆的高度,丁同学建议换用一个质量为50克钢球。你认为应当采用的建议。
主题Ⅰ:探究氯化钠样品中杂质的成分
已知所提供的氯化钠样品中,可能含有硫酸钠、氯化镁、氯化钙中的一种或几种杂质。甲同学的实验探究过程记录如下:
根据以上实验信息,甲同学得出结论:此氯化钠样品中含有的杂质是硫酸钠。
【实验分析】
主题Ⅱ:测定氯化钠样品中氯化钠的质量分数
【提出问题】该固体的成分是什么?
【查阅资料】①Cu是紫红色固体 ②Cu2O是红色固体 ③Cu2O+H2SO4(稀)=CuSO4+Cu+H2O
【猜想与假设】
猜想一:Cu 猜想二:Cu、Cu2O 猜想三:Cu、C 猜想四:Cu、Cu2O、C
小晨同学认为猜想不正确,因为反应后的固体不完全是紫红色。
【实验探究】
实验操作 | 实验现象 | 实验结论 |
步骤一:取少量固体置于烧杯中,加入足量稀硫酸,观察溶液颜色 | 溶液呈色 | 猜想三不正确 |
步骤二:把步骤一中所得混合物过滤,将滤渣干燥后置于滤纸上,观察固体颜色 | 固体为紫红色、黑色 | 猜想正确 |
【实验反思】由于受反应物质量比、反应物接触面积和反应温度等因素的影响,固体物质之间的反应可能无法完全进行。
【拓展延伸】
①从理论上看,碳与氧化亚铜的质量比应为1:12,但实际做实验时却将碳与氧化亚铜的质量比控制在约1:10,这样操作的理由是。
②下列可以用于鉴别真、假黄金的方法是(填字母)。
A.观察颜色 B.加热固体 C.滴加稀硫酸 D.滴加硝酸银溶液

【提出问题】HDPE膜由什么元素组成?
【查阅资料】①HDPE膜能够燃烧,燃烧可能生成一氧化碳;②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
【实验探究】如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D(装置中每步反应均进行完全)。

【实验记录】
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
【实验分析】
【查阅资料】①糯米中加入食用碱可起到中和微生物生成的酸、软化食物纤维等作用;
②草木灰中富含钾盐,主要成分是K2CO3 , 还含有少量K2SO4和KCl。
【实验探究】检验草木灰的成分,并测定草木灰中K2CO3的质量分数。

为进步确定滤液中所含溶质的成分,他们进行了以下实验探究。
猜想二:NaOH和Na2CO3;
猜想三:;
猜想四:NaOH、Na2CO3、Ca(OH)2
经过分析,大家一致认为上述猜想四不需要验证,肯定是错误的,原因是(用化学方程式表示)。
【实验探究】
方案一:取一定量的滤液于试管中,往其中滴加少量稀盐酸,无明显实验现象。
方案二:取一定量的滤液于另一试管中,往其中滴加氯化钡溶液,观察到有白色沉淀产生。
【讨论交流】根据实验现象,得出猜想是正确的。请解释方案一中无明显现象的原因是。
样品中CaH2的质量分数为多少?(写出计算过程)