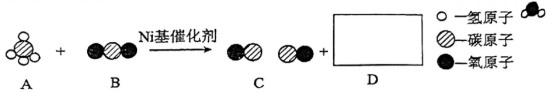
 B .
B .  C .
C .  D .
D . 
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 点燃 |
| B | N2 | O2 | 通过灼热的铜粉 |
| C | CaO | CaCO3 | 加适量的水,过滤 |
| D | CuO | C | 隔绝空气加强热 |
随着工业生产的高速发展和人们生活水平的提高,排入大气中的CO2越来越多,导致温室效应增强。碳替代、碳减排、碳封存、碳循环是实现碳中和的四种主要途径。科学家预测,到2050年,四种途径对全球碳中和的贡献率如图1。CO2的吸收是碳封存的首要环节,常选用NaOH、氨水、一乙醇胺等作吸收剂。在研究膜吸收法吸收CO2时,研究人员通过实验比较了一乙醇胺、二乙醇胺、氨基乙酸钾三种吸收剂对烟气中CO2的脱除效果,其结果如图2。
依据上文,回答下列问题:

回答下面实验问题:

a.用锌粒与稀硫酸反应制氢气
b.用石灰石与稀盐酸反应制二氧化碳
c.用过氧化氢和二氧化锰制氧气
d.加热无水醋酸钠和碱石灰固体混合物制甲烷
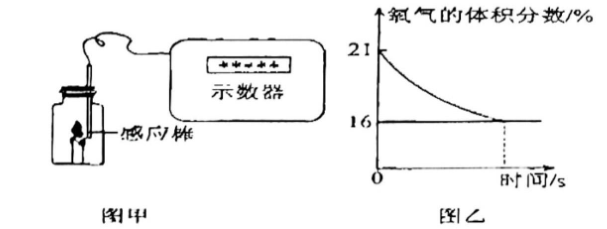
如图是901班化学实验小组对“燃烧的条件”实验活动的部分操作示意图


金属 | 钛(Ti) | 铝(Al) | 钒(V) |
熔点/℃ | 1668 | 660 | 1919 |
钛合金是用要的航空材料,可用来制造航空发动机的叶片等。若将上表中几种金属融合制成钛合金,该合金的熔点是( )