

酞菁分子中所有原子共平面,其中轨道能提供一对电子的
原子是(填图2酞菁中
原子的标号)。钴酞菁分子中,钴离子的化合价为,氮原子提供孤对电子与钴离子形成键。


回答下列问题:
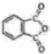 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(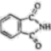 )都是合成菁的原料,后者熔点高于前者,主要原因是。
)都是合成菁的原料,后者熔点高于前者,主要原因是。
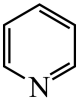 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的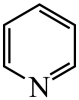 、
、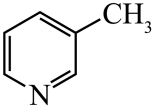 、
、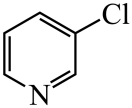 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。
物质 | HCON(CH3)2 | HCONH2 |
相对分子质量 | 73 | 45 |
沸点/℃ | 153 | 220 |
HCON(CH3)2的相对分子质量比HCONH2的大,但其沸点反而比HCONH2的低,主要原因是。
物质 | CF4 | SiF4 | BF3 | AlF3 |
熔点/℃ | -183 | -90 | -127 | >1000 |
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,原因是。
过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用,回答下列问题:
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar] 3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
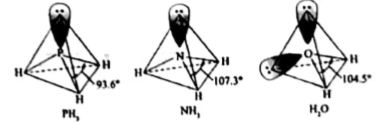
PH3中P的杂化类型是, NH3的沸点比PH3的,原因是。H2O的键角小于NH3的,分析原因。
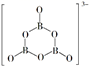
在该反应中,B原子的杂化轨道类型由变为。

氨硼烷晶体的密度ρ=g·cm−3(列出计算式,设NA为阿伏加德罗常数的值)。
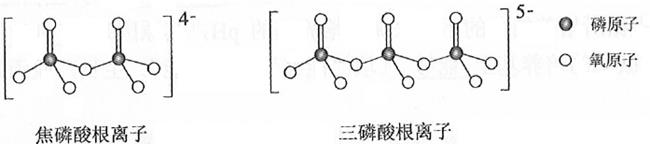
这类磷酸根离子的化学式可用通式表示为(用n代表P原子数)。
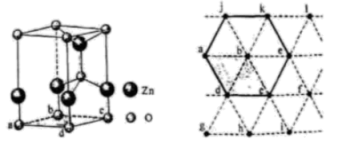
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
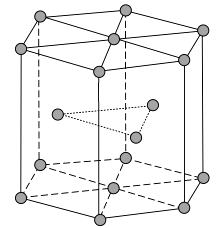
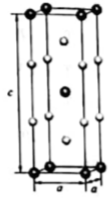
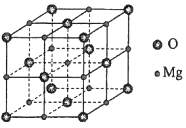
MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2﹣)为nm.MnO也属于NaCl型结构,晶胞参数为a'=0.448nm,则r(Mn2+)为nm.
元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1).第二周期部分元素的E1变化趋势如图(a)所示, 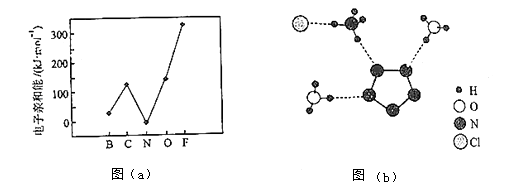
其中除氮元素外,其他元素的E1自左而右依次增大的原因是;氮元素的E1呈现异常的原因是.
①从结构角度分析,R中两种阳离子的相同之处为,不同之处为.(填标号)
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
②R中阴离子N5﹣中的σ键总数为个.分子中的大π键可用符号Πmn表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为Π66),则N5﹣中的大π键应表示为.
③图(b)中虚线代表氢键,其表示式为(NH4+)N﹣H…Cl、、.