 B . 棉纱织布
B . 棉纱织布  C . 木材燃烧
C . 木材燃烧  D . 汽油挥发
D . 汽油挥发 
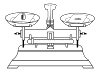 称量氯化钠
B .
称量氯化钠
B . 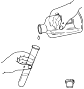 倾倒液体
C .
倾倒液体
C . 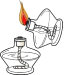 点燃酒精灯
D .
点燃酒精灯
D . 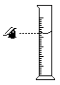 读取液体体积
读取液体体积
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约三分之一体积的NaCl溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaCl反应 |
| B | 用玻璃棒取少量待测液滴在湿润的pH试纸上,与标准比色卡对照并读出待测液的pH | pH试纸显示pH=1对应的红色 | 待测液显酸性 |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯。 | 烧杯内壁有无色液滴产生 | 该气体一定是CH4 |
①妈妈为爸爸斟了满满一杯白酒,小红远远就闻到了酒的特殊香味,请从微观的角度解释能闻到香味的原因;爸爸点燃了生日蜡烛。许愿后大家一起将蜡烛吹灭。这种熄灭蜡烛火焰的原理是。
②小红用压岁钱给爸爸买了一条羊毛围巾。日常生活中可以用的方法检验羊毛纤维和合成纤维;妈妈说面粉是制作蛋糕的主要原料,面粉中富含的营养素为。
①所得溶液是20℃时氯化钠的溶液(填“饱和”或“不饱和”)
②20℃时,氯化钠的溶解度为g.
①需要质量分数为12%的氯化钠溶液mL(计算结果精确到0.1),需要水mL(水的密度为1g/cm3).
②该溶液配制过程中用到的仪器除了量筒、烧杯玻璃棒外,还需要量取所需要的12%的氯化钠溶液时,应选用(填“10mL”或“20mL”或“50mL”)规格的量筒.
③把配制好的上述溶液装入中(填“广口瓶”或“细口瓶”),盖好瓶塞并贴上标签.