
①面条是以面粉为原料制作而成的。面粉的主要成分淀粉[化学式为(C6H10O5)n]是可以燃烧的,淀粉充分燃烧的产物是;面粉燃烧过程中可闻到烧焦羽毛气味,是因为面粉中还含有的营养物质是。
②为避免面粉厂车间发生爆炸事故,生产过程可采取的措施有。
A.密封门窗,隔绝氧气
B.严禁吸烟,杜绝火源
C.轻拿轻放,减少粉尘扬起
D.提高面粉的着火点
③优质的面粉来自优良的小麦。为了提高生长期小麦的抗倒伏能力,需施加肥。
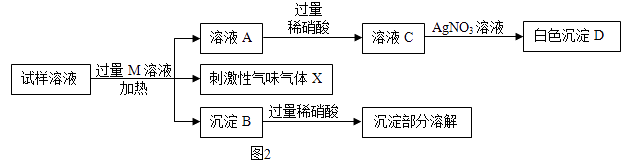
①白色沉淀D的化学式是。
②试样溶液加入过量M溶液时生成X的化学反应方程式是。
③根据以上实验可以判断该试样溶液中一定含有上述五种物质中的(写化学式)。

①空气反应器中,金属镍与氧气在一定条件下燃烧生成氧化镍(NiO);燃料反应器中发生的部分化学反应如下:Ⅰ.H2+NiO Ni+H2O;Ⅱ.CO+NiO
Ni+CO2 , 其中属于置换反应的是(填“Ⅰ”或“Ⅱ”),反应Ⅱ中发生还原反应的物质是。
②与CO、H2直接在空气中燃烧相比,化学链燃烧排放出的CO2浓度更高的原因是。
①吸收池内生成碳酸氢钠的化学方程式是。
②合成塔内生成甲醇的化学反应中,参加反应的H2与CO2的质量比是。该反应中,原料H2的理想来源是。如果将来H2的制取技术取得突破,“CO2与H2反应高效变甲醇”这一世界领先的研究成果的意义是(答出一条即可)。
查阅资料:Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4=CuSO4+Cu+H2O
【猜想假设】红色粉末是①Cu②Cu2O③
实验步骤 | 实验现象 | 实验结论 |
取红色粉未于试管中,加人足量稀硫酸 | 红色粉末中含有Cu2O |
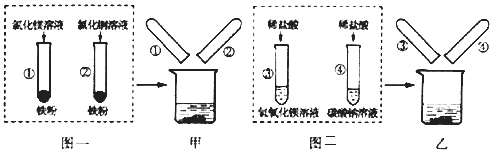
实验操作 | 实验现象 | 实验结论 |
步骤1:取少量滤液于试管中,向其中滴加足量硝酸钡溶液, | 有白色沉淀生成 | ①生成的白色沉淀是(写 化学式,下同) ②滤液中的溶质共有哪些 |
步骤2:静置,向上层清夜中滴加无色酚酞试液 | 溶液变红 |
查阅资料:
①氨气水溶液呈碱性
②浓硫酸和碱石灰都可做气体吸收剂;浓硫酸能吸收氨气,不能吸收二氧化碳;碱石灰是氧化钙与氢氧化钠固体的混合物,不与氨气反应。
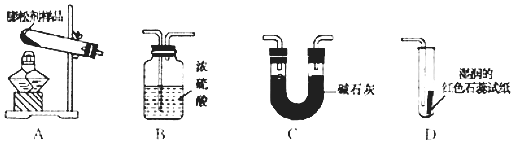
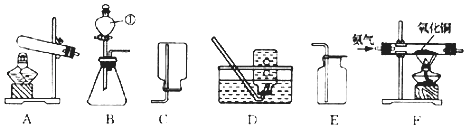
依次连接A、C、D装置,点燃A处的酒精灯,将试管中的该膨松剂样品充分加热至完全反应后,通过观察到、现象可以证明该膨松剂中含有NaHCO3和 NH4HCO3两种物质。其中装置C的作用是。
序号 | 实验操作 | 测得数据 |
实验1 | 将其中的一份膨松剂样品加入A装置试管中,将A装置依次连接 B、C装置,充分加热至膨松剂完全反应 | 装置C增重1.98g |
实验2 | 将另一份膨松剂样品加人A装置试管中,将A装置依次连接 C、B装置,充分加热至膨松剂完全反应 | 装置B增重0.34g |
基于以上实验数据分析,该品牌膨松剂中 NaHCO3和 NH4HCO3的质量比是。