①酸性氧化物在一定条件下均能与碱发生反应
②金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
③蔗糖和硫酸钡均属于电解质
④盐酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
⑤因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
⑥氢氧化铁胶体稳定存在的主要原因是胶粒直径介于1~100nm
| 选项 | 甲 | 乙 |
| A |
|
|
| B |
|
|
| C |
|
|
| D |
|
|
选项 | 家务劳动 | 化学知识 |
A | 用白醋除去水壶中的水垢 | 白醋可溶解 |
B | 用小苏打粉作膨松剂焙制糕点 |
|
C | 用含NaClO的84消毒液拖地 | NaClO有还原性 |
D | 用洁厕灵洗马桶 | 洁厕灵中含有盐酸,可以与尿垢反应 |

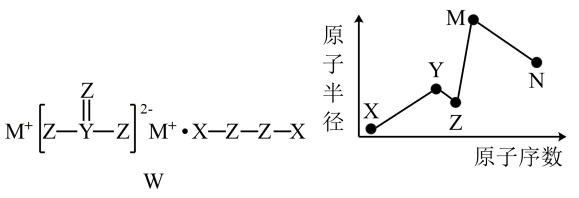
①属于二元酸,写出它与
反应生成酸式盐的化学方程式;
②与
溶液反应生成的酸式盐只有一种,则
是元酸;若反应生成正盐,则该正盐的化学式为。

已知:常温下极不稳定,为易溶于水但不与水反应的易挥发、易爆气体,沸点11℃。
①产物中
的化合价是。
②以和
为原料,制得
和
, 反应的化学方程式为。
③盛放仪器的名称为,冰水浴的作用是。
④产物气被集气瓶B中盛放的稳定剂(某混合盐溶液)吸收,稳定剂的作用是。
⑤烧杯中混合液的作用是吸收尾气,试配平离子方程式:
。
成分 | 质量(g) |
蔗糖(C12H22O11) | 25.000 |
硫酸钾 | 0.870 |
阿司匹林 | 0.180 |
高锰酸钾 | 0.316 |
硝酸银 | 0.075 |

①;②。

①沉淀减少时发生的离子方程式:。
②a点的数值为:mL。