
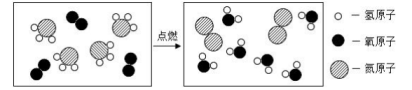


请回答:
【提出问题】铁制品锈蚀与哪些因素有关?
【查阅资料】Ⅰ.氯化钙固体可作干燥剂。Ⅱ.常温常压,氢气密度是0.089g/L。
Ⅲ.一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
【设计与实验】
龙龙:定性探究铁锈蚀的因素
取洁净无锈铁钉分别放入试管(A、B、C试管中为相同的普通铁钉,D试管中为纯铁钉),进行图1实验,一段时间后,观察到A铁钉表面有铁锈,B、C、D铁钉表面无明显现象。

装置如图2所示,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,t1时刻加入2mL饱和NaCl溶液后,t3时刻再将一只装有5mL稀盐酸的注射器插到烧瓶上,采集数据如图3、图4。

据图3,0-t2时刻说明铁在生锈过程中(填“吸收”或“放出”)热量。

【查阅资料】:
①氧化铜经一氧化碳还原不仅能生成铜,还可能生成中间产物氧化亚铜(Cu2O);
②Cu2O是不溶于水的红色固体,能与酸发生反应,生成Cu2+和Cu。
【提出猜想】:氧化铜经一氧化碳还原所得到的红色固体中除Cu外还可能含有Cu2O。
【进行实验】:小明根据所查阅的资料,设计了一个最简单的实验方案:取少量该红色固体放入盛有的试管中,振荡,若出现的现象,则说明还含有Cu2O。
【设计与实验】同学们设计并进行如图所示实验(实验中所用金属均已用砂纸打磨)。

实验Ⅰ中只有一支试管内有气泡产生,反应的化学方程式为。
由上述实验得出三种金属活动性由强到弱的顺序是锌、铜、银。
某同学又取了金属M放入试管中,滴加稀硫酸,发现有气泡产生,请你推测:金属M(填“能”或“不能”)与硫酸铜溶液发生化学反应。
同学们用不同形状的锌和不同溶质质量分数的稀硫酸在室温下进行实验,探究锌与稀硫酸反应快慢的影响因素,实验记录表:
实验编号 | 硫酸的溶质质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
实验①②对比说明;要比较不同溶质质量分数的稀硫酸对反应快慢的影响,应选择的实验编号是。
由此得出锌的形状和稀硫酸的溶质质量分数都会影响反应快慢。