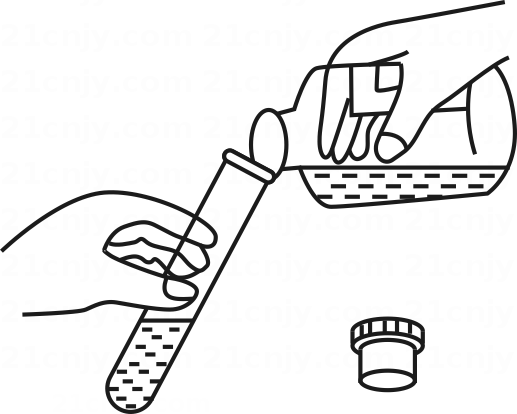
 加入液体
B .
加入液体
B .  稀释浓硫酸
C .
稀释浓硫酸
C . 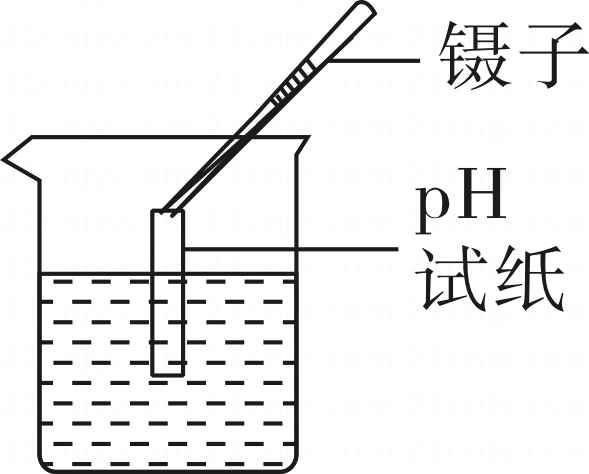 测量pH
D .
测量pH
D . 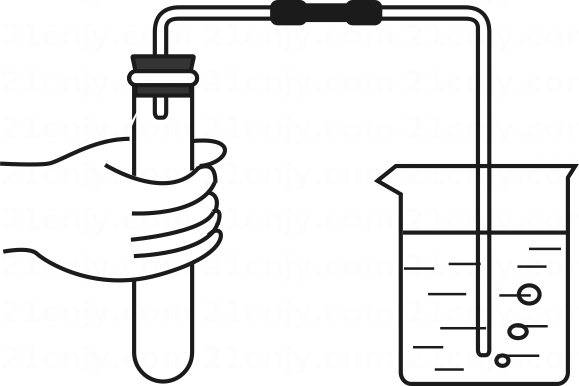 检验气密性
检验气密性

 B .
B .  C .
C .  D .
D . 

| 试剂甲 | 试剂乙 | |
| A | NaCl | AgNO3 |
| B | H2SO4 | Ba(OH)2 |
| C | HCl | NaOH |
| D | K2CO3 | HNO3 |
①常用降低土壤酸性的是;
②区别稀盐酸和稀硫酸的物质;
已知:氯化氢(HCl)是极易溶于水的无色气体,其水溶液俗称盐酸。
 B .
B .  C .
C .  D .
D . 


实验 组别 | 球质量/克 | 球释放高 度/厘米 | 图钉起始插 入深度/厘米 | 图钉碰撞后 深度/厘米 |
① | 5 | 50 | 0.5 | 2.5 |
② | 15 | 50 | 0.5 | 6.5 |
③ | 20 | 50 | 0.5 | 8.5 |
④ | 5 | 40 | 0.5 | 2.1 |

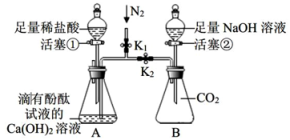
步骤1:打开活塞①,逐滴滴加稀盐酸直至过量后关闭活塞①;同时打开K1 , 鼓入N2(起搅拌作用,使反应充分进行)。
步骤2:关闭K1 , 打开活塞②,将足量NaOH溶液注入锥形瓶后立即关闭活塞②。
步骤3:一段时间后,打开K2。
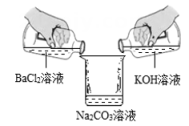
【猜想与假设】甲:Na+、Ba2+、K+、OH-、Cl-
乙:Na+、CO32-、K+、OH-、Cl-
丙:Na+、CO32-、Ba2+、K+、OH-、Cl-
丁:Na+、K+、OH-、Cl-


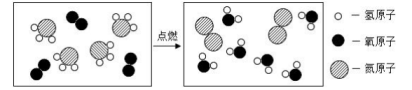
①盐酸是氯化氢气体溶于水形成的水溶液,在盐酸中存在氢离子、氯离子和水分子。
②氯化氢气体也可溶于甲苯(一种有机溶剂),氯化氢的甲苯溶液中氯化氢以分子的形式存在。盐酸与氯化氢的甲苯溶液的微观示意图如图1所示。
③为此,向盛有NaHCO3粉末的试管中通入HCl气体,无明显现象;停止通气后,再加入少量水,试管内则反应生成气体。
④紫色石蕊滴加入盐酸溶液而变红,紫色石蕊加入氯化氢的甲苯溶液中无明显现象。


| 硝酸铵(NH4NO3)5% 磷酸钠(Na3PO4) 10% 硫酸钾(K2SO4) 5% |
|
时间/分 |
0 |
2 |
4 |
6 |
8 |
10 |
|
C 瓶溶液增加的质量/g |
0 |
3.0 |
5.0 |
6.0 |
6.6 |
6.6 |

