 斩竹漂塘
B .
斩竹漂塘
B .  煮楻足火
C .
煮楻足火
C .  汤料入帘
D .
汤料入帘
D .  覆帘压纸
覆帘压纸
 B . 探究甲烷中是否含碳元素
B . 探究甲烷中是否含碳元素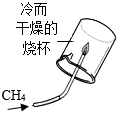 C . 验证质量守恒定律
C . 验证质量守恒定律 D . 比较铁、铝金属活动性
D . 比较铁、铝金属活动性
 B . 纯棉毛巾
B . 纯棉毛巾 C . 涤纶运动服
C . 涤纶运动服 D . 青铜古剑
D . 青铜古剑
A.机械能 B.化学能 C.热能

品名 | 豌豆黄 |
主要原料 | 豌豆 |
主要营养成分 | 蛋白质、糖类、钠、钙、钾、镁、铁等元素 |
①“豌豆黄”中主要含有蛋白质、糖类和三类营养素。
②“豌豆黄”中含有钙元素,人体缺钙常会引起。(填字母序号)
A.贫血症 B.侏儒症 C.甲状腺肿大 D.佝偻病
③“豌豆黄”中含有的人体所需微量元素是。

在A实验结束后①、②试管内的物质倒入废弃物烧杯中,发现烧杯中的红色固体物质明显增多,一段时间后过滤,同学们向滤渣中滴加稀盐酸,发现没有气泡产生,那么滤液中可能含有的溶质是。
(一)锌的广泛应用
锌被称之为“生命元素”。儿童、青少年如果缺锌严重,将会导致侏儒症和智力发育不良。
A.金属材料 B.无机非金属材料
C.合成材料 D.复合材料

| 沉淀物 | Fe(OH)3 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 6.2 | 6.3 |
| 完全沉淀pH | 3.2 | 8.0 | 9.7 |
为加快“溶解池”中的反应速度,可采取的措施是。
实验一:探究单质钙
【问题】钙的化合物很多,为什么我们很少提起单质钙呢?
【猜想】钙的化学性质活泼。
【资料】
①微溶于水,溶解能力随着温度的升高而降低,其水溶液呈碱性。
②在一个化学反应中,有元素化合价升高,可时就有元素化合价降低。
【实验验证】


工业上可以用鸡蛋壳制备过氧化钙CaO2 , 该活动小组设计图3装置,通过测定生成O2的体积,计算样品中CaO2的质量分数。
已知:①;②杂质不与盐酸反应;③量气管有刻度值,且0刻度在上。
图3整套装置的气密性检验方法:。