A.10mL量筒 B.20mL量筒 C.50mL量筒 D.胶头滴管



A.减少汽车的保有量
B.用风能与太阳能发电替代燃煤发电
C.减少工业生产中二氧化碳的排放


①变化I、Ⅱ、Ⅲ中属于化学变化的是。
②N经变化Ⅲ到M需要一定的外界条件,该条件可能是。
③在R、M、N三个框图中,能表示混合物的是。(填字母序号)

研究发现,同种元素的原子核中,中子数不一定相同,如氢元素的原子核(如下表)。
氧元素的原子核 | 原子名称 | |
质子数(Z) | 中子数(N) | |
1 | 0 | 氕 |
1 | 1 | 氘 |
1 | 2 | 氚 |
为了更好地区别同种元素的不同原子,常用原子符号来表示质量数为A,质子数为z的X原子,其中质量数=质子数+中子数。如上述氕、氘、氚3种不同的氢原子就可以依次表示为
.质子数相同而中子教不同的同一元素的不同原子互称为同位素。如
互为同位素。同位素在生活、生产和科学研究中有着重要用途。例如考古时利用
测定一些文物的年代;通过测定
和
, 分析古代人类的食物结构:追踪
发出的射线,确定磷在植物中的作用部位等。
A 原子的结构示意图为
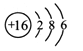
B 氘原子与氚原子的相对原子质量不同
C 由和
组成的1个水分子中含11个中子
D 氕、氘、氚3种氢原子最多可以组成6种不同的氢分子

A.收集前集气瓶中要装满水
B.为了避免浪费,加热前先将导气管伸入到集气瓶口
C.收集的氧气不纯的原因只能是装置气密性不好
D.实验结束后应先将导管移出水面,再停止加热
【猜想与假设】
I.氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变:
II.氧化铜参与了反应产生氧气,反应前后质量和化学性质发生改变:
III.氧化铜是反应的催化剂,反应前后。
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下图实验:

①请补充能证明猜想Ⅲ成立的实验现象:步骤③现象为,步骤⑥中二氧化锰固体质量为g。结论:猜想成立。
②步骤①的目的是。
③定性判断步骤①和步骤②的反应快慢,可根据。
④过氧化氢能被CuO催化分解放出氧气的符号表达式为。
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
II.取30粒含MnO2的海藻酸钠微球,采用如图2所示装置进行实验。改用其他三种微球,分别重复上述实验,得到如图3所示的锥形瓶内压强随时间变化的曲线图。

每次实验时,海藻酸钠微球数应相同的目的是。