|
共价键 |
H-H |
I-I |
H-I |
|
键能/kJ·mol−1 |
436 |
151 |
299 |
则该反应的ΔH=kJ·mol−1。
②下列叙述能说明上述反应已达到平衡的是。
a.单位时间内生成nmolH2 , 同时生成nmolHI
b.温度和体积一定时,HI浓度不再变化
c.温度和体积一定时,混合气体颜色不再变化
d.温度和压强一定时,混合气体的密度不再变化
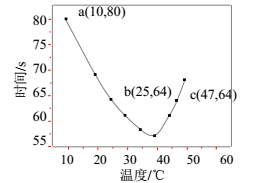
图中a点对应的NaHSO3反应速率为mol·L-1·s-1。b、c两点对应的NaHSO3反应速率v(b)v(c)(填“>”、“=”、“<”)。
NH4I(s)=NH3(g)+HI(g)①
2NH3(g)=N2(g)+3H2(g)②
2HI(g)=I2(g)+H2(g)③
达平衡时,体系中n(HI)=bmol,n(I2)=cmol,n(H2)=dmol,则n(N2)=mol,t℃时反应①的平衡常数K值为 (用字母表示)。