①常温下,将丙溶液加水稀释,下列数值一定变小的是(填字母)。
A. B.
C.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙甲(填“>”“<”或“=”)。
②相同条件下,取等体积、等pH的Ba(OH)2、NaOH和NH3∙H2O三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为、
、
, 则三者的大小关系为。
③某温度下,测得0.001mol/L的HCl溶液中水电离出的c(H+)=1×10-9mol∙L-1 , 将VaLpH=4HCl溶液和VbLpH=9的Ba(OH)2溶液混合均匀,测得溶液的pH=7,则Va:Vb=。
弱电解质 | H2SO3 | H2CO3 | HClO | NH3∙H2O |
电离平衡常数 |
①将SO2通入氨水中,当c(OH-)降至1.0×10-7mol∙L-1时,溶液中的=。
②下列微粒在溶液中不能大量共存的是。
A.、
B.
、
C.
、
D.
、
Ⅰ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 , 图中的离子交换膜只允许
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,电极质量减少
。
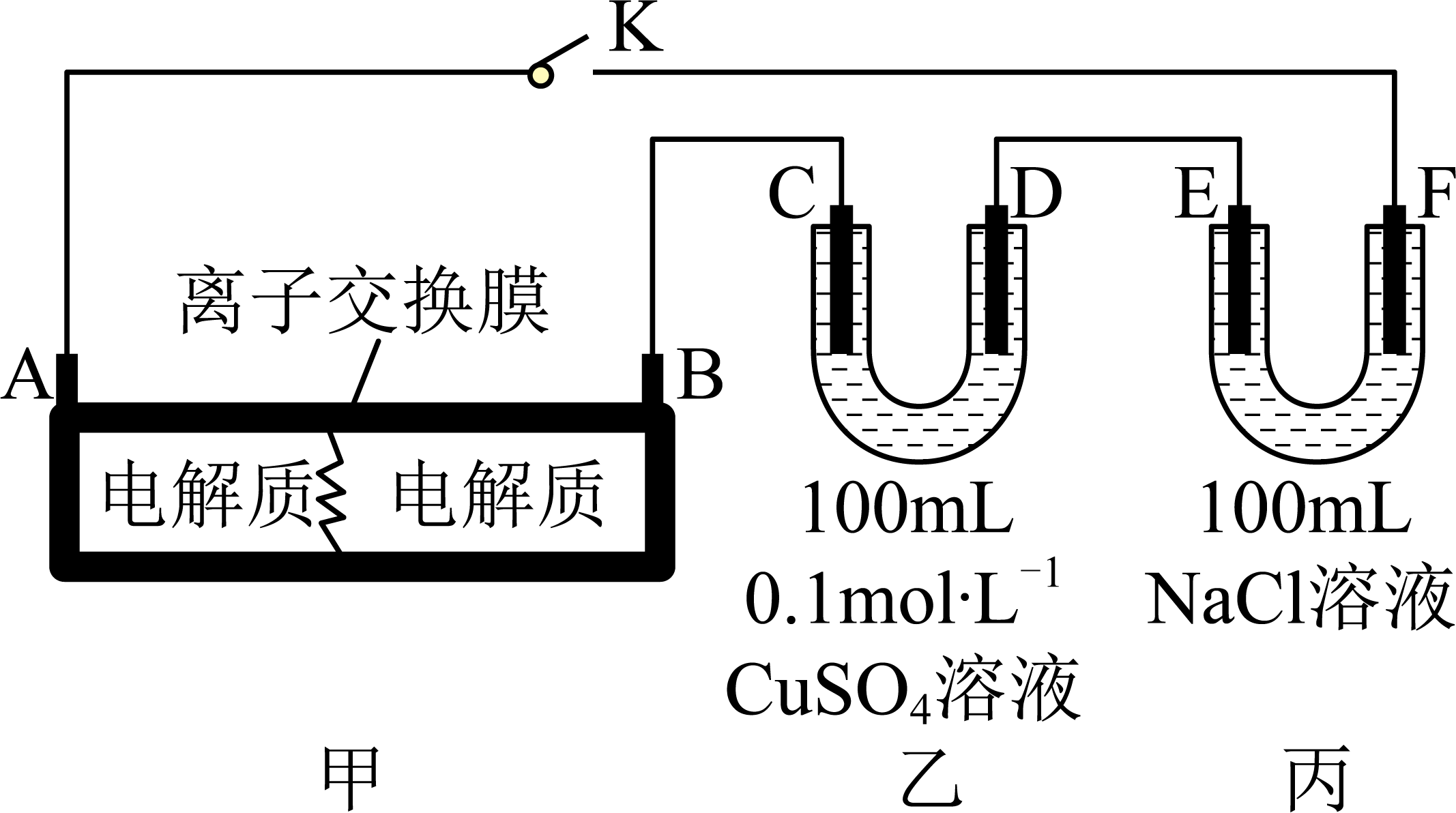
Ⅰ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 , 图中的离子交换膜只允许
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,电极质量减少
。



Y离子交换膜为(填“阳”或“阴”)离子交换膜。
反应Ⅰ:
反应Ⅱ:
回答下列问题:


反应Ⅰ:
反应Ⅱ:
则反应。

A.的消耗速率和
的消耗速率相等
B.混合气体的密度不再发生变化
C.容器内气体压强不再发生变化
②图中表示时
的物质的量分数随温度变化关系的曲线是(填字母),理由是;在N点所示条件下,
反应达到平衡,平衡时容器的体积为L,反应Ⅱ的
。(以分压表示,分压=总压×物质的量分数)
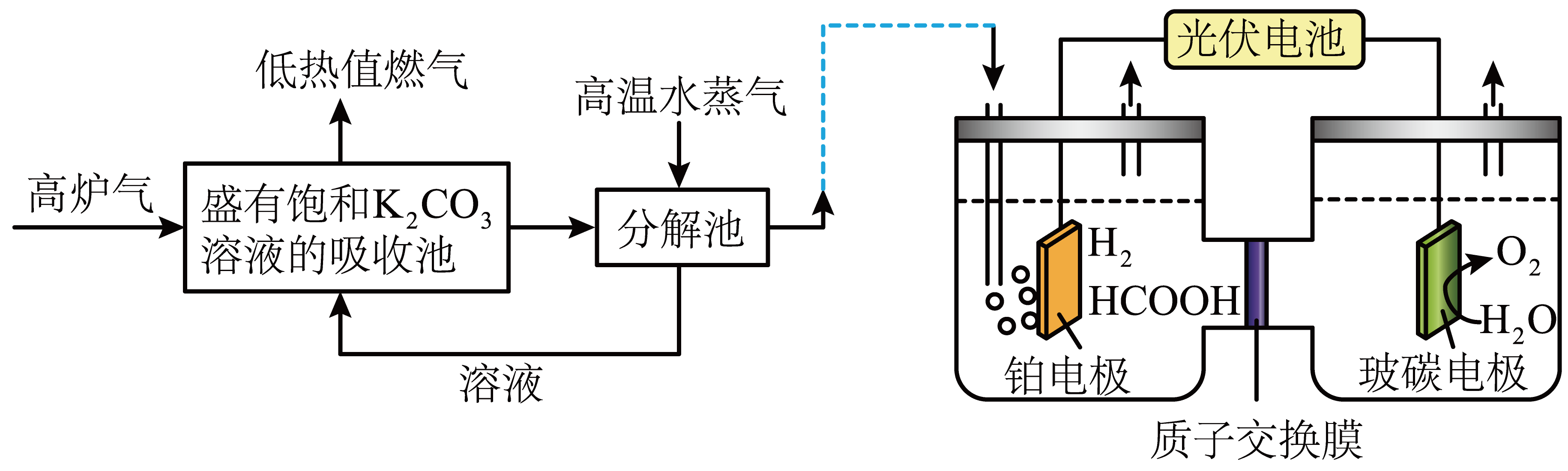
①某温度下,当吸收池中溶液的时,此时该溶液中
[已知:该温度下
,
]。
②利用电化学原理控制反应条件能将电催化还原为
, 电解过程中还伴随着析氢反应,若生成
的电解效率为80%,当电路中转移
时,阴极室溶液的质量增加g。[B的电解效率=
]。