Ⅰ:
Ⅱ:
请回答:
A.低温低压B.低温高压C.高温低压D.高温高压

①下列说法正确的是。
A.可循环利用,
不可循环利用
B.过程ⅱ,吸收
可促使
氧化
的平衡正移
C.过程ⅱ产生的最终未被
吸收,在过程ⅲ被排出
D.相比于反应Ⅰ,该流程的总反应还原需吸收的能量更多
②过程ⅱ平衡后通入 , 测得一段时间内
物质的量上升,根据过程ⅲ,结合平衡移动原理,解释
物质的量上升的原因。
①常压下和
按物质的量之比
投料,某一时段内
和
的转化率随温度变化如图1,请在图2中画出
间R的变化趋势,并标明
时R值。

②催化剂X可提高R值,另一时段内转化率、R值随温度变化如下表:
|
温度/℃ |
480 |
500 |
520 |
550 |
|
|
7.9 |
11.5 |
20.2 |
34.8 |
|
R |
2.6 |
2.4 |
2.1 |
1.8 |
下列说法错误的是
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中占比越高
C.温度升高,转化率增加,
转化率降低,R值减小
D.改变催化剂提高转化率,R值不一定增大
已知:①含锌组分间的转化关系:
②是
的一种晶型,
以下稳定。
请回答:
用(称量样品
)→用烧杯()→用( )→用移液管()→用滴定管(盛装
标准溶液,滴定
)
仪器:a、烧杯;b、托盘天平;c、容量瓶;d、分析天平;e、试剂瓶
操作:f、配制一定体积的Zn2+溶液;g、酸溶样品;h、量取一定体积的溶液;i、装瓶贴标签
某研究小组取人血浆铜蓝蛋白(相对分子质量
),经预处理,将其中
元素全部转化为
并定容至
。取样测得荧光强度比值为10.2,则1个血浆铜蓝蛋白分子中含个铜原子。

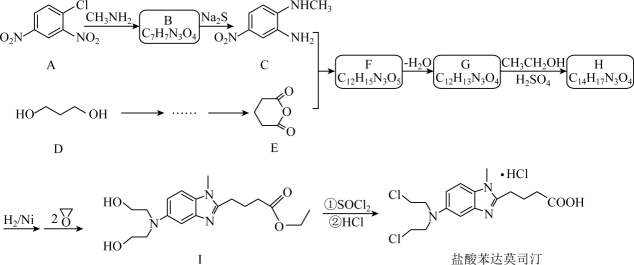
已知:①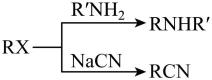
②
请回答:
①分子中只含一个环,且为六元环;②谱和
谱检测表明:分子中共有2种不同化学环境的氢原子,无氮氮键,有乙酰基
。