 B . 滴加液体
B . 滴加液体 D . 闻气体气味
D . 闻气体气味

①冰刀鞋中含有的金属材料是。
②铝虽然较活泼,但抗腐蚀性能好,原因是。

选项 | 甲 | 丙 | 丁 |
A | Mg | Al | Fe |
B | Fe | Al | Cu |
C | Mg | Fe | Al |
D | Mg | Fe | Cu |
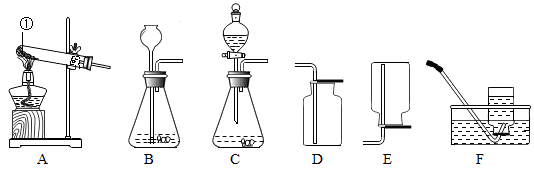
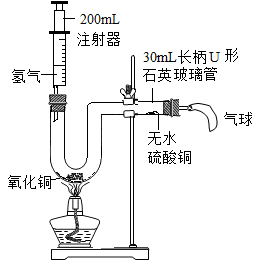
①为确保实验安全,在点燃酒精灯加热前的操作是。
②装置末端连接的气球的作用是。
③实验过程中,当观察到现象时可判断一定有产物水生成。
【查阅资料】84消毒液的有效成分是次氯酸钠,化学式为NaClO。
【实验】取少量84消毒液置于试管中,滴加H2O2溶液,有大量气泡产生,经检验产生的气体为氧气。
【提出问题】在上述反应中,NaClO的作用是什么?
猜想一:NaClO与H2O2溶液发生反应,作反应物
猜想二:NaClO类似分解H2O2溶液制取氧气时MnO2的作用,作。
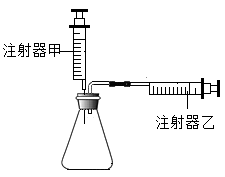
用注射器甲向锥形瓶中压入5mL水,若观察到注射器乙的活塞向右移动5mL,则说明该装置。
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
H2O2溶液/mL | 5 | 5 | 5 | 5 | 5 |
注射器乙中气体的总体积/mL | 35 | 70 | 85 | a | b |