
已知:①“青矾”是指 , 高温受热可完全分解得红棕色固体和气体混合物;
②熔点-75.5℃,沸点-10℃:
熔点16.8℃,沸点44.8℃。
请回答下列问题:
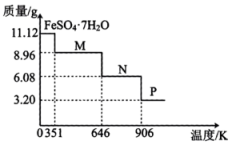
A装置中发生反应的化学方程式为。
在装置C中先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入流速一致。四次实验分别得到如表pH-t图:
① | ② | ③ | ④ |
已煮沸的 | 未煮沸的 | 已煮沸的 | 未煮沸的 |
|
|
|
|
C装置中覆盖食用油的目的是。

写出实验室制备苯甲酸乙酯的化学方程式。
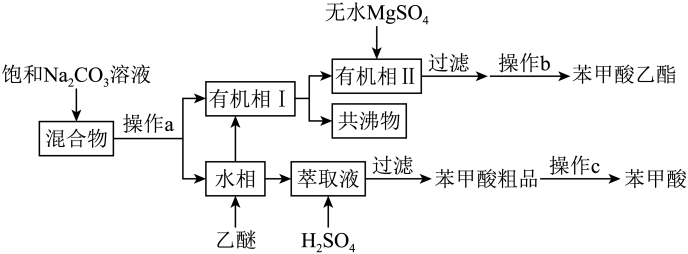
已知:环己烷沸点为80.8℃;乙醚的密度为0.834g/cm3 , 沸点34.5℃;乙醚-环己烷-水共沸物的沸点为62.1℃。
向混合物中加入饱和Na2CO3溶液的目的是。

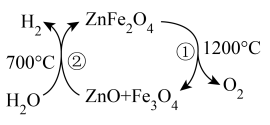
I.以作催化剂,采用“
催化加氢制甲醇”方法将其资源化利用。反应历程如下:
i.催化剂活化:(无活性)
(有活性);
ii.与
在活化的催化剂表面同时发生如下反应:
①主反应:
,
②副反应:
。
b.某温度下,与
的混合气体以不同流速通过恒容反应器。气体流速增大可减少产物中
的积累,从而减少催化剂的失活,请用化学方程式表示催化剂失活的原因:。

升高温度,反应的化学平衡常数(填“增大”或“减小”或“不变”)。
a.在230℃以上,升高温度的平衡转化率增大,但甲醇的产率降低,原因是。
b.在300℃发生反应,反应达平衡时,的转化率为50%,容器体积减小20%。则反应②用平衡分压表示的平衡常数Kp=(保留两位有效数字)。
i.
ii.
上述反应中为吸附活性炭,反应历程的能量变化如图1所示:

干重整反应的速率由决定(填“反应i”或“反应ⅱ”),
干重整反应的热化方程式为。(选取图1中
、
、
表示反应热)。