 B .
B .  C .
C . 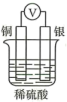 D .
D . 

A.=15mL B.=35mL C.<15mL D.>35mL

②根据消耗的NaOH溶液的量,计算该葡萄酒中含量为
。
②利用装置A进行实验,发现锌片、锰片质量均减轻,说明装置中除了发生电化学反应,还发生非电化学反应,该反应的离子方程式为。实验结束时测得电解质溶液增加32.8g,电流表中有1mol电子发生转移,则锌溶解了g。
②若装置B中负极金属的消耗速率为 , 则盐桥中K+的迁移速率为
。
①若加稀释至相同的
, 则溶液中加入
的体积:
(填“>”、“<”或“=”)
。
②若加稀释相同的倍数,则此时溶液的
(填“>”、“<”或“=”)
。
①溶液中(填“增大”、“减小”、“不变”或“无法判断”)。
②滴加溶液至溶液中的
, 此时溶液的
(填“>”、 “<”或“=”)7,判断的理由为。

请回答下列问题: