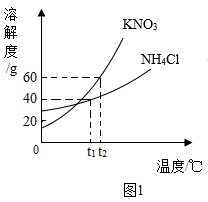

①t1℃时,氯化铵的溶解度为。
②烧杯Ⅱ中KNO3溶液的溶质质量分数为。
③下列关于图2中烧杯内物质的说法正确的是(填字母)。
A.烧杯Ⅲ中溶液的质量是160g
B.烧杯Ⅱ、Ⅲ、Ⅳ中,只有Ⅳ中上层清液是饱和溶液
C.若使烧杯Ⅳ中的固体溶解,可采用加水或升温的方法
D .烧杯Ⅳ的上层清液中溶质质量分数一定比Ⅱ的溶液中溶质质量分数大
④若用溶质质量分数为16%的氯化铵溶液和蒸馏水来配制100 g溶质质量分数为10%的氯化铵溶液,则所需16%的氯化铵溶液与蒸馏水的质量比为。
写出实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式。用向上排空气法收集二氧化碳的原因是。
①选择适当的反应,包括;
②选择合适的;
③验证所制得的气体。
A.氢氧化钠溶液 B.碳酸氢钠溶液 C.硝酸银溶液
【查阅资料】
①二氧化碳与水、碳酸钙能通过化合反应生成碳酸氢钙,碳酸氢钙可溶于水。
②电导率传感器用于测量溶液的导电性强弱,相同温度下同种溶液离子浓度越大,电导率越大。
③浊度传感器用于测量溶液中悬浮物的多少,悬浮物越多则透光率越小,浊度值越小,溶液透明时浊度值(透光率)为100%。
【实验验证】
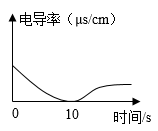
该同学将制得的二氧化碳持续通入少量澄清石灰水中,用电导率传感器釆集数据,如图所示。

【分析推理】
实验中0~10 s澄清石灰水变浑浊、溶液电导率降低的原因是(用化学方程式表示)。
若同时使用浊度传感器测定反应过程中澄清石灰水浑浊的情况,反应过程中溶液浊度与时间变化的曲线如图,下列说法错误的是_______(填字母)。
