
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
下列判断正确的是( )
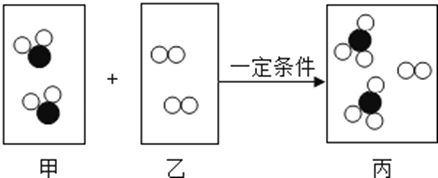
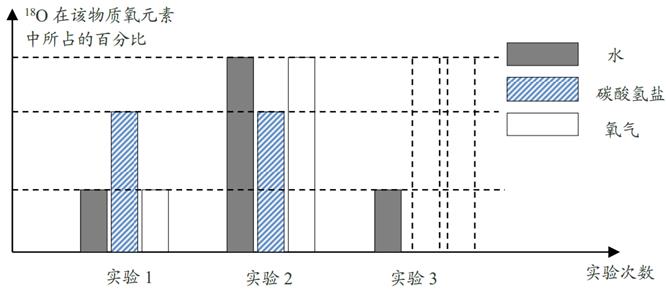
资料:I.在相同的温度和压强下,相同体积的气体具有相同的分子数。
II.18O的相对原子量为 18,16O的相对原子量为 16。
III.自然界的氧气在标准状况下的密度为1.43 kg/m3 , 16O 占所有氧原子的比例可近似看作 100%。
查阅资料:人体骨骼中的钙存在形式是羟基磷酸钙[Ca10(PO4)6(OH)2],该物质难溶于水。人体平均每天需要补钙 800mg。
|
氮肥 |
化学式 |
每千克的售价 |
|
硝酸铵 |
NH4NO3 |
10元 |
|
尿素 |
CO(NH2)2 |
16元 |
根据表格回答计算分析问题(写出计算过程,保留2个有效数字):
|
氮肥(硝酸铵) (NH4NO3) 硝酸铵含量>95% 净重:50Kg 含氮量:34.3% |